胃癌免疫抑制新机制!复旦大学附属中山医院/上海交通大学医学院附属第九人民医院:改善转移患者预后的新治疗靶点
| 导读 | 靶向细胞外基质驱动的免疫抑制机制,可能是克服这种侵袭性疾病治疗耐药性并提高免疫治疗效果的一种有前景的策略。 |
3月9日,复旦大学附属中山医院/上海交通大学医学院附属第九人民医院研究团队合作共同在期刊《Journal for ImmunoTherapy of Cancer》上发表了研究论文,题为“Hyaluronic acid-CD44 signaling defines therapeutic resistance and immunosuppressive microenvironment in peritoneal metastasis of gastric cancer”,本研究结果表明,透明质酸 - CD44 信号传导是胃癌腹膜转移中细胞外基质重塑与免疫逃逸之间的重要联系。靶向细胞外基质驱动的免疫抑制机制,可能是克服这种侵袭性疾病治疗耐药性并提高免疫治疗效果的一种有前景的策略。
胃癌腹膜转移预后差,透明质酸作用机制成破局关键
01
胃癌(GC)是全球第五大常见癌症,也是全球癌症死亡的第三大原因。腹膜转移(PM)是胃癌最常见的转移类型,由于治疗效果不佳,腹膜转移患者的预后约为 3 至 9 个月。过去二十年中,靶向转移性胃癌的几种全身性疗法已被引入,但进展有限,因为血浆 - 腹膜屏障的存在以及腹膜转移的血供不良限制了全身性药物的组织渗透和治疗效果。这凸显了阐明腹膜扩散的分子机制以及确定新的治疗靶点的迫切需求。
腹膜转移微环境的一个关键特征是其独特的细胞外基质(ECM),其中透明质酸(HA)已成为一个关键调节因子。透明质酸合成的增加会提高基质的密度和硬度,从而增强间质压力,并促进肿瘤细胞在间皮表面的黏附、迁移和存活。从机制上讲,透明质酸与 CD44、LYVE1 和 ICAM1 等特定受体相互作用,激活多个下游信号通路,促进上皮间质转化和血管生成。除了其结构作用外,富含透明质酸的基质还充当物理和生化屏障,限制药物扩散并改变免疫细胞活性。然而,透明质酸在胃癌腹膜扩散中的具体作用及其潜在机制仍不清楚。
靶向 CD44 可减轻调节性 T 细胞介导的免疫抑制,并增强抗 PD-1 免疫疗法在胃癌腹膜转移中的疗效
02
为探究 CD44+ 调节性 T 细胞(Tregs)在多发性肌炎(PM)免疫抑制效应中的潜在作用,研究人员研究了 CD44+ Tregs 的数量是否会影响免疫治疗的效果。选取了 12 名接受过免疫治疗的皮肌炎(PM)患者,不出所料,“部分缓解”(PR)患者的生存率高于“疾病稳定/疾病进展”(SD/PD)患者。其中,PR 患者的 CD44+ Tregs、PD1+ 细胞比例较低,CD8+ 细胞比例较高。为进一步探究抗 CD44 与抗 PD1 联合使用是否能减轻 Treg 介导的免疫抑制,将 C57 小鼠随机分为四组,接受图中提及的不同治疗。在不同时间点监测肿瘤生长情况。有趣的是,抗 CD44 与抗 PD1 联合使用减少了小鼠腹部肿瘤结节的数量,同时 CD4+ T 细胞(包括 Tregs)、PD1+ 细胞数量减少,CD8+ 细胞数量增加。总之,抗 CD44 与抗 PD1 联合治疗显示出比单药治疗更强的疗效。最后,将这些发现整合到一个机制示意图中表明,透明质酸与 CD44 的结合会招募 IQGAP1 并激活 RAC1,进而使 SMAD3 磷酸化,从而驱动 FOXP3 转录和调节性 T 细胞分化,从而促进免疫抑制和肺间质纤维化。
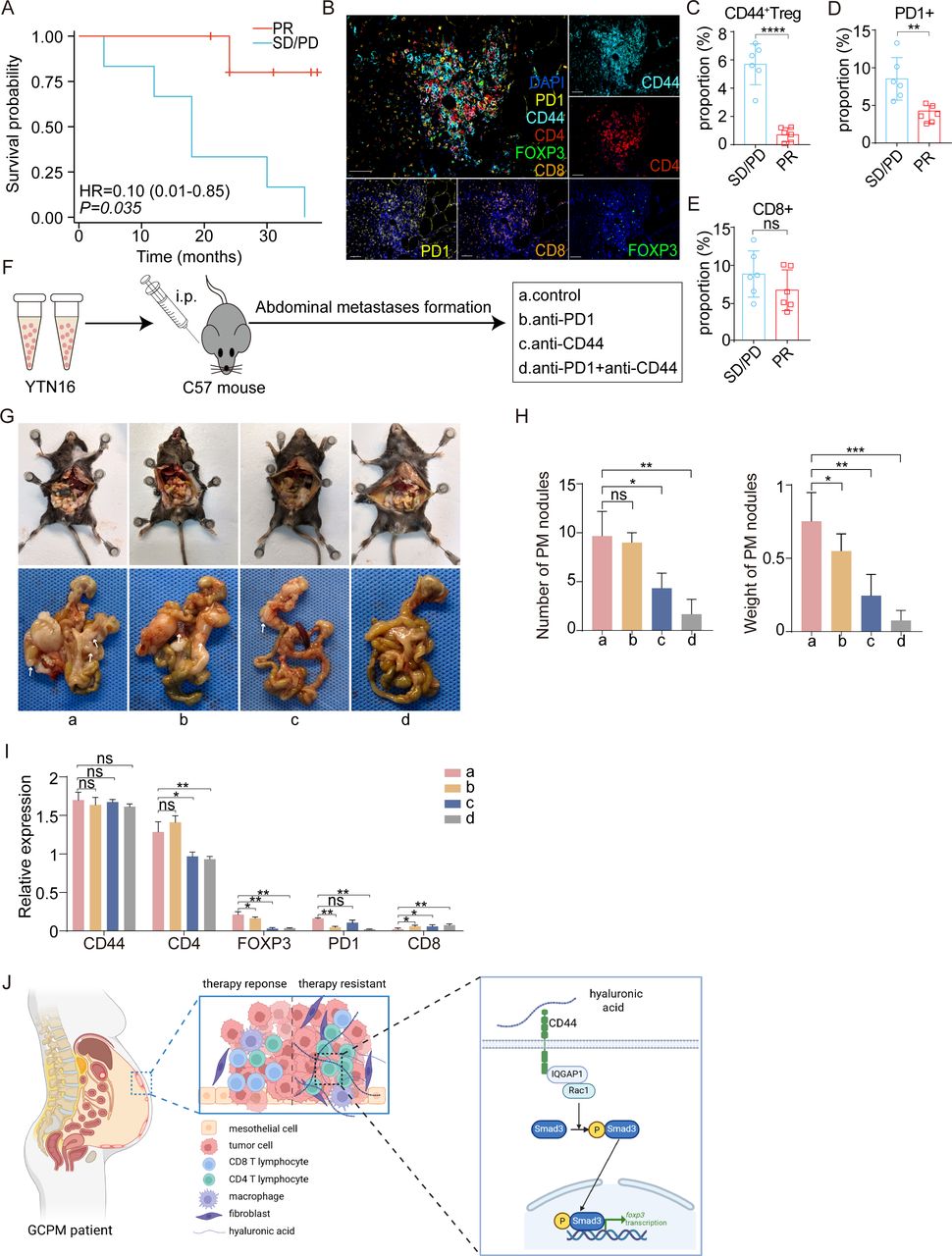
CD44+ 调节性 T 细胞与免疫治疗耐药相关,联合 CD44/PD-1 阻断可增强腹膜转移的治疗效果
结论
03
本研究结果为将细胞外基质靶向策略与免疫疗法相结合提供了机制依据。这些发现不仅加深了对透明质酸 - CD44 轴与免疫微环境之间复杂相互作用的理解,而且为将透明质酸或 CD44 作为克服免疫抑制和增强免疫疗法在这一具有挑战性疾病的疗效的策略提供了强有力的临床前依据。
参考资料:
https://jitc.bmj.com/content/14/3/e014179(转化医学网360zhyx.com)
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
责任声明:本稿件如有错误之处,敬请联系转化医学网客服进行修改事宜!
微信号:zhuanhuayixue
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发